NCS- Idade x Fertilidade; infertilidade; diferenciação sexual; Fecundação natural e in vitro
- 16 de dez. de 2020
- 15 min de leitura
1ano 1 semestre 2módulo 3SP
08 de Abril de 2019

PROBLEMAS:
O uso prolongado do anticoncepcional
Adiamento da gravidez
Oligospermia
3 tentativas falhas
2 anos sem engravidar após parar de utilizar o anticoncepcional
HIPÓTESES:
A partir dos 35 anos: endométrio refratário, cito II envelhecidos dificultando a fecundação, divisão celular prejudicada.
Gestante idosa: 45 anos (A partir do 35 anos)
O uso prolongado de anticoncepcional --> cte progesterona + estrógeno -- feedback negativo--> alta queda de FSH --> atrofia do ovário --> infertilidade
Após o uso prolongado da pílula leva até 1 ano para voltar a fertilidade
Dificuldades de uma fecundação natural: pH vaginal, trajetória ( canal vaginal, colo do útero ( muco), útero, tuba uterina, ampola, dissolver a zona pelúcida)
Vantagens da fertilização in vitro, evitar as dificuldades a cima
± 80% de chance de engravidar pelo método natural
Infertilidade: incapacidade de fecundação natural dentro de 2 anos tentando 3x por semana
Principais causas de infertilidade: tabagismo, álcool, uso de drogas, uso de anabolizantes, genética. Exclusividade feminina: endometriose, ovário policístico, mioma, idade, câncer de colo de útero, hostilidades, anatomia do útero e questões emocionais
A diferenciação sexual é devida ao cromossomo Y ( SRY)
Hipóteses confirmadas: A (parcialmente), C, E, F, I, J
Hipóteses refutadas: B, H,
QUESTÕES
Como a idade influência na fertilidade e na gravidez? A,B
Como/Por que o uso prolongado de anticoncepcional influência na fertilidade? C
Quanto tempo leva para restabelecer a fertilidade após a interrupção do uso da pílula anticoncepcional? D
Compare a fecundação natural com relação a in vitro em termos de mecanismo e a sua eficácia E, F, G
Conceitue infertilidade e quais são suas principais causas? H, I
Como ocorre a diferenciação sexual? J
RESPOSTAS
QUESTÃO 1
As mulheres nascem com todos os óvulos que elas irão ter por toda vida. Dos 1.000.000 de óvulos que uma recém-nascida tem ao nascimento, apenas 300.000 restam no momento que ela alcança a puberdade. Deste número, apenas em torno de 300 óvulos serão ovulados durante os anos reprodutivos da mulher... na taxa de um óvulo por mês. Geralmente, as mulheres são mais férteis na casa dos 20 anos, então a fertilidade começa a declinar à medida que ela vai atingindo o final de seus 20 anos. É importante saber que após os 35anos de idade, as chances de uma mulher ter um bebê naturalmente declinam em média em 50%. Após os 40 anos, as chances diminuem em torno dos 90%. Assim que a menopausa se aproxima, as capacidades reprodutivas da mulher vão diminuindo e se tornam menos efetivas em produzir óvulos maduros e saudáveis. À medida que a mulher envelhece e chega próximo à menopausa, seus ovários já não respondem bem aos hormônios que são responsáveis por ajudar na ovulação.
A menina na puberdade inicia as suas menstruações com cerca de 300 mil óvulos disponíveis nos seus ovários e a cada ciclo menstrual, para um óvulo que atinge a ovulação, mil são perdidos, fazendo que ao redor dos 50 anos dificilmente existam óvulos capazes de serem fecundados.
Dessa forma a mulher se torna praticamente incapaz de engravidar com os próprios óvulos. É o fim do estoque de óvulos disponíveis para serem fertilizados, o fim da “reserva ovariana”.

CURIOSIDADE:
AVALIAÇÃO DA RESERVA OVARIANA
A Reserva Ovariana é avaliada, fundamentalmente, pela dosagem sanguínea de quatro hormônios no 3º dia do ciclo menstrual: FSH, estrogênio, inibina-B e hormônio anti-mulleriano além da ultrassonografia no início do ciclo menstrual.
FSH maior do que 10 mlU/ml e estrogênio maior que 35 pg/ml, geralmente sugerem uma má respondedora aos estímulos hormonais (“Poor Responder”).
FSH menor do que 10 mlU/ml e estrogênio menor do que 35 pg/ml geralmente sugerem uma boa respondedora aos estímulos hormonais (“Good responder”).
Inibina-B: é um hormônio fabricado pelas células dos ovários e indica a quantidade de óvulos disponíveis para serem fertilizados. Quando estiver com concentração abaixo do normal, significa que existe uma diminuição deste número e a capacidade de engravidar está também, teoricamente, menor.
Hormônio anti-mulleriano(AMH): É um hormônio fabricado por células do ovário(folículos) e dá uma ideia do número de óvulos existentes nos ovários capazes de serem fertilizados no presente e, para o futuro, a possível longevidade reprodutiva.
ULTRASSONOGRAFIA: avalia o tamanho, o volume dos ovários e a presença de folículos iniciais (ou folículos primordiais). Ovários pequenos e sem estes folículos significa uma Baixa Reserva Ovariana.
MENOPAUSA/CLIMATÉRIO
Nos países ocidentais, na maioria das mulheres a menopausa ocorre entre 45 anos a 56 anos, situando-se a média de 51 anos, o período de transição da fase procriativa para a não procriativa.
OBS.:
-A menopausa e o envelhecimento não se apresentam de forma padronizada em todas as mulheres.
-A menopausa dá-se quando o número de folículos se situa abaixo de um limiar crítico, cerca de 1.000, independentemente da idade.
A perimenopausa, que dura de dois a cinco anos, configura o momento em que o corpo feminino sofre mudanças fisiológicas que resultarão na menopausa. Basicamente, o que ocorre nesse período e culmina na menopausa é a baixa de produção do hormônio estrogênio pelos ovários e as glândulas suprarrenais, tornando a menstruação irregular, com menor fluxo do que antes e um tempo mais longo entre os períodos menstruais.
Perimenopausa ou climatério é um termo utilizado para descrever o período em que se manifestam os primeiros sintomas ou indicadores da proximidade da menopausa e que termina 12 meses após a última menstruação. Esta período de transição tem duração variável de mulher para mulher, caracterizando-se por alterações dos níveis das hormonas esteroides ováricas que se exprimem, por um lado, por alterações do ciclo menstrual e, lógica típica, sobretudo vasomotora.
A menopausa – interrupção fisiológica dos ciclos menstruais devido ao fim da secreção hormonal dos ovários – é o termo mais conhecido da etapa de transição da vida da mulher. Esse período é definido como “quando uma mulher para de ovular e não pode mais procriar” e tem, geralmente, apontado como marco a última menstruação.
Para a Organização Mundial de Saúde (1996), tem-se a definição desse período da seguinte forma: A menopausa é a fase da vida da mulher que cessa a capacidade reprodutiva. Os ovários deixam de funcionar e a produção de esteroides e peptídeo hormonal diminui e consequentemente se produzem no organismo diversas mudanças fisiológicas, algumas resultantes da função ovariana e de fenômenos menopáusicos a ela relacionados e outros devido ao processo de envelhecimento. Quando se aproxima da menopausa, muitas mulheres experimentam certos sintomas, em geral passageiros e inócuos, porém não menos desagradáveis e às vezes incapacitantes
NOVA SÍNTESE:
Redução nas praticas de implantação (nidação mais difícil), aborto espontâneo, má qualidade e menor quantidade de oócitos, maior probabilidade de alterações comossômicas, aumento de pré eclâmpicia, maior risco de diabetes gestacional, mortalidade do feto . EX: 20 ANOS : 1/1667 e 45 ANOS: 1/30
REFERÊNCIAS:
Clínica de Fertilidade e Reprodução Humana - https://fertilidade.org/content/idade-e-fertilidade-feminina
Revista bimestral de ciência e investigação em saúde - http://biblioteca.isave.pt/publicacoes/revistas/SER_SAUDE_6.pdf
Ferreira, V. N., Chinelato, R. S. C., Castro, M. R., & Ferreira, M. E. C. (2013). Menopausa: marco biopsicossocial - http://www.scielo.br/pdf/psoc/v25n2/18.pdf
Brasil. Ministério da Saúde. Secretaria de Atenção à Saúde. Departamento de Ações Programáticas Estratégicas. Manual de Atenção à Mulher no Climatério/Menopausa / Ministério da Saúde, Secretaria de Atenção à Saúde, Departamento de Ações Programáticas Estratégicas. – Brasília : Editora do Ministério da Saúde, 2008. 192 p. – (Série A. Normas e Manuais Técnicos) (Série Direitos Sexuais e Direitos Reprodutivos – Caderno, n.9) - http://bvsms.saude.gov.br/bvs/publicacoes/manual_atencao_mulher_climaterio_menopausa.pdf
Águas, Fernanda - Menopausa - http://www.fspog.com/fotos/editor2/cap_18.pdf
QUESTÃO 2
Among ever users of OCs, we found that OC use for longer time periods was associated with increased fecundability and young age at the first OC use was associated with reduced fecundability compared with initiation of OC use after the age of 21.
Although we adjusted for cycle irregularity and heaviness of flow, decreased fecundability could occur if young women used OCs for therapeutic reasons and these problems persisted after OC cessation.
Several biological mechanisms may explain our findings. OCs prevent ovulation by suppressing hypothalamic and pituitary secretion of hormones (Dickey, 2007), which may influence both the short-term delay in fecundability after OC discontinuation and improved fecundability after long-term OC use. A residual hormonal effect influencing ovulation after OC cessation could lead to the short-term delay in fecundability
Specifically, recent OC use was associated with lower cervical mucus quality, later estimated date of ovulation and decreased intensity of menstrual flow (a marker for quality of endometrial lining) (Nassaralla et al., 2011). A long-term use of OCs might increase fertility by inhibiting follicle depletion over a woman's reproductive life. This hypothesis seems plausible as levels of the anti-Mullerian hormone, a clinical marker of ovarian reserve, have been found to be stable with extended OC use (Somunkiran et al., 2007; Steiner et al., 2010). Moreover, some studies have shown that OCs postpone the depletion of the follicle pool and delay natural menopause (Gold et al., 2001; Palmer et al., 2003).
Women who have used OCs for 4 years or more should be reassured because we found no evidence that long-term OC use deleteriously affects fecundability. Like short-term users, long-term users appear to experience a short-term delay in getting pregnant compared with those discontinuing barrier methods. The association between young age at first OC use and reduced fecundability is notable, but may partially reflect early age at first use among women with cycle irregularities.
Compared with barrier methods, the use of OCs as the last contraception method before attempting to conceive was associated with a short-term delay in return of fertility (FR = 0.87, 95% CI: 0.79–0.96).
Longer term OC use was associated with higher fecundability: compared with OC use for less than 2 years;
FRs were 0.98 (95% CI: 0.83–1.15) for 2–3 years,
1.16 (95% CI: 0.98–1.37) for 4–5 years,
1.10 (95% CI: 0.93–1.29) for 6–7 years,
1.17 (95% CI: 0.99–1.38) for 8–9 years,
1.23 (95% CI: 1.04–1.46) for 10–11 years
1.28 (95% CI: 1.07–1.53) for ≥12 years of OC use.
NOVA SÍNTESE:
Com o uso por mais de 2 anos ---> inibição de FSH ---> Menor desenvolvimento folicular ---> Deprime a função ovariana (atrofia) --->infertilidade tem.
REFERÊNCIAS:
a Danish prospective cohort study (Estudo Coorte Prospectivo Dinamarquês) - Ellen M. Mikkelsen Anders H. Riis Lauren A. Wise Elizabeth E. HatchKenneth J. Rothman Henrik Toft Sørensen - Human Reproduction, Volume 28, Issue 5, May 2013, Pages 1398–1405, - ttps://academic.oup.com/humrep/article/28/5/1398/940795
OBS.:
The use of third and fourth generation OCs was associated with longer TTP (time to pragnancy) compared with the use of second generation OCs.
We found that progestin type was associated with TTP; users of third and fourth generation OCs had longer TTPs compared with second generation OC users.
Pílulas de primeira geração
A primeira geração da pílula contracetiva tinha uma concentração mais elevada de estrogénio e progesterona. As versões artificiais da hormona progesterona encontradas nas pílulas de primeira geração incluíam noretinodrel, noretindrona, lynestrol e diacetato de etinodiol.
A primeira geração da pílula estava relacionada com alguns problemas de saúde, muito devido à quantidade de hormonas usadas. As pílulas mais recentes utilizam uma dose mais baixa de ambas as hormonas. As pílulas de primeira geração já não se encontram disponíveis em Portugal.
Pílulas de segunda geração
As pílulas de segunda geração tornaram-se disponíveis nos anos 70 e tinham uma quantidade ainda mais baixa de hormonas. Estas contêm progesterona como o levonorgestrel e a noretisterona. Muitas pílulas atualmente prescritas contêm estas hormonas. As pílulas de segunda geração mais frequentemente prescritas atualmente são a Microginon, a Logynon e a Loestrin.
Pílula de terceira geração
Uma década após o lançamento das pílulas de segunda geração, apareceu a terceira geração de pílulas. Este grupo de pílulas usa progesteronas como o norgestimato, o desogestrel, o gestodeno e o acetato de ciproterona. As pílulas de terceira geração estão disponíveis sujeitas a receita médica e incluem a Cilest e a Marvelon.
Pílulas de quarta geração
O tipo mais recente de pílulas contracetivas contém progesteronas como a drospirenona, o acetato de nomegestrol ou o dienogest. As pílulas deste grupo incluem a Yasmin (que contém etinilestradiol e drospirenona), a Zoely (com hemi-hidrato de estradiol e acetato de nomegestrol) e a Qlaira (com valerato de estradiol e dienogest).
QUESTÃO 3
Ao fazer a interrupção da pílula, o corpo começa a se preparar para a ovulação novamente. Os hormônios que antes eram da pílula não estão mais presentes, e o corpo precisa começar a produzi-los sozinho. Quando esse processo se inicia – o que normalmente pode levar de dois a três meses – a ovulação e a menstruação devem voltar ao normal.
NOVA SÍNTESE:
Oral, adesivo e anel vaginal - 2 ou 3 ciclos para normalizar o ciclo menstrual
Implante e injetável - 6 a 9 meses para normalizar o ciclo menstrual
Sistema liberador de levonorgestrel (DIU ) - imediato, contido pode levar até 2 ciclos
REFERÊNCIAS:
07/12/2015 - NACE - https://nace.igenomix.com.br/blog/em-quanto-tempo-posso-engravidar-apos-parar-com-o-anticoncepcional/
QUESTÃO 4
Fecundação Natural
Sequência da fecundação
Normalmente o local da fecundação é ampola da tuba uterina .se o oócito não for fecundado na ampola ele passa lentamente pela tuba e chega ao corpo do útero, onde se degenera e é reabsorvido.
Embora fecundação possa ocorrer em outras partes da tuba, ela não ocorre no corpo do útero.
Sinais químicos (químiotaxia) secretados pelo oocitos e pelas células foliculares guiam os espermatozoides capacitados para o oócitos
A fecundação começa com o contato entre o espermatozoide e oócito 2 e termina com a mistura dos cromossomos maternos e paternos na metáfase da primeira divisão mitótica do zigoto (embrião unicelular)
O processo de fecundação leva aproximadamente 24 horas
FASES DA FECUNDAÇÃO
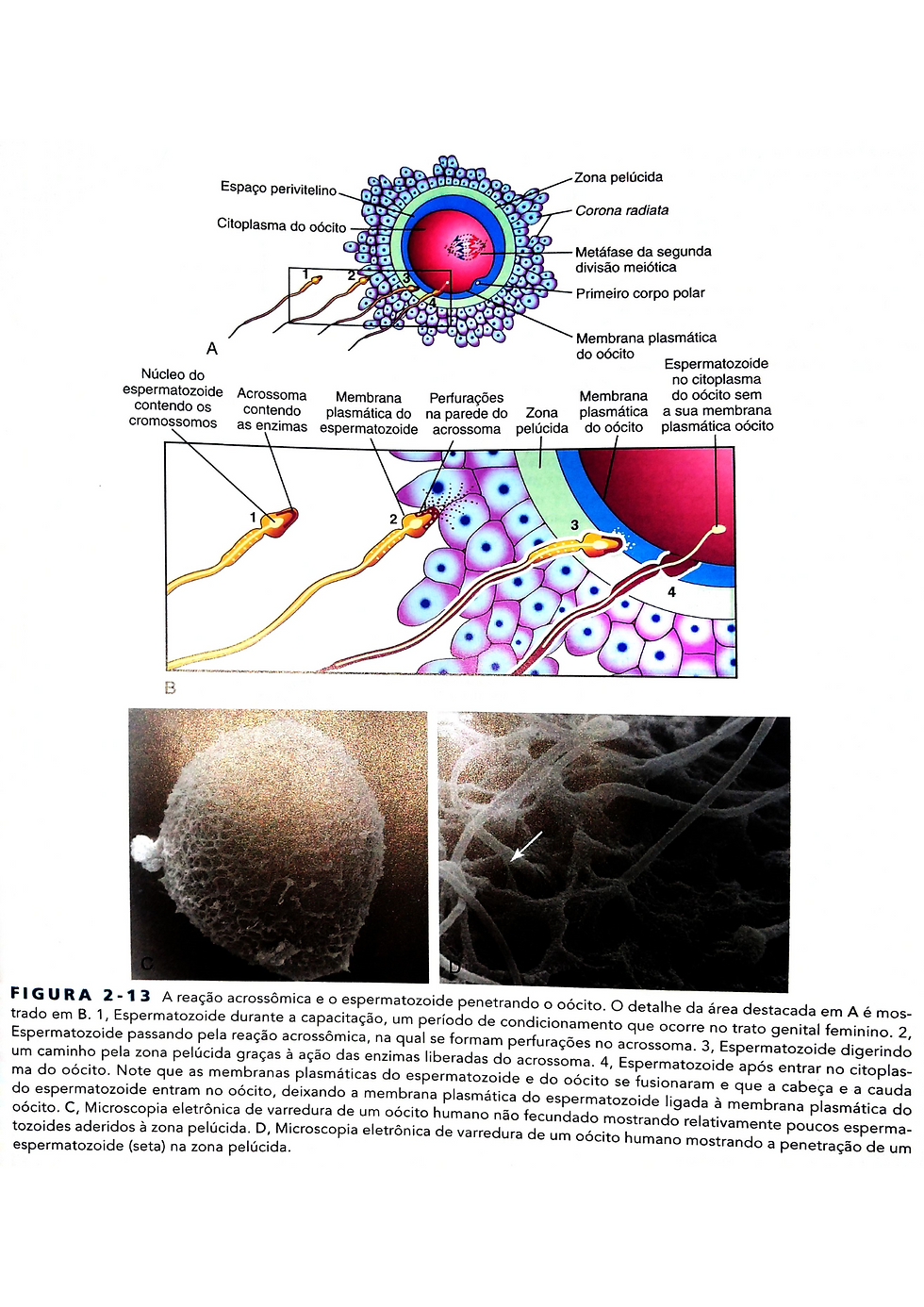
1- passagem de um espermatozoide através da da corona radiata. A dispersão das células foliculares parece resultar principalmente da ação da enzima e hialuronidase liberada da vesícula acrossômica do espermatozoide. Algumas enzimas da mucosa da tuba uterina também auxiliam na dispersão.
2- penetração da zona pelúcida. Fase mais importante, as enzimas esterase, acrosina e neuramidase parecem causar a lise (dissolução) da zona pelúcida, formando assim uma passagem para o espermatozoide penetrar o cito 2
3- Uma vez que o espermatozoide penetra a zona pelucida ocorre a reação zonal ,uma alteração nas propriedades da zona pelúcida, tornando-a impermeável a outros espermatozoides. Essa reação é o resultado da ação de enzimas lisossomais liberadas por grânulos corticais próximos a membrana plasmática do oócitos. O conteúdo desses grânulos que são liberados no espaço perivitelino, também provoca alterações na membrana plasmática tornando-a impermeável aos outros espermatozoides.
4- fusão das membranas plasmáticas do ovócito e do espermatozóide. as membranas plasmáticas ou celulares do oócito e do espermatozóide se fundem se rompem na região da fusão. a cabeça e a cauda do espermatozóide entram no citoplasma do oócito, mas a membrana celular espermática (membrana plasmática) e as mitocôndrias não entram.
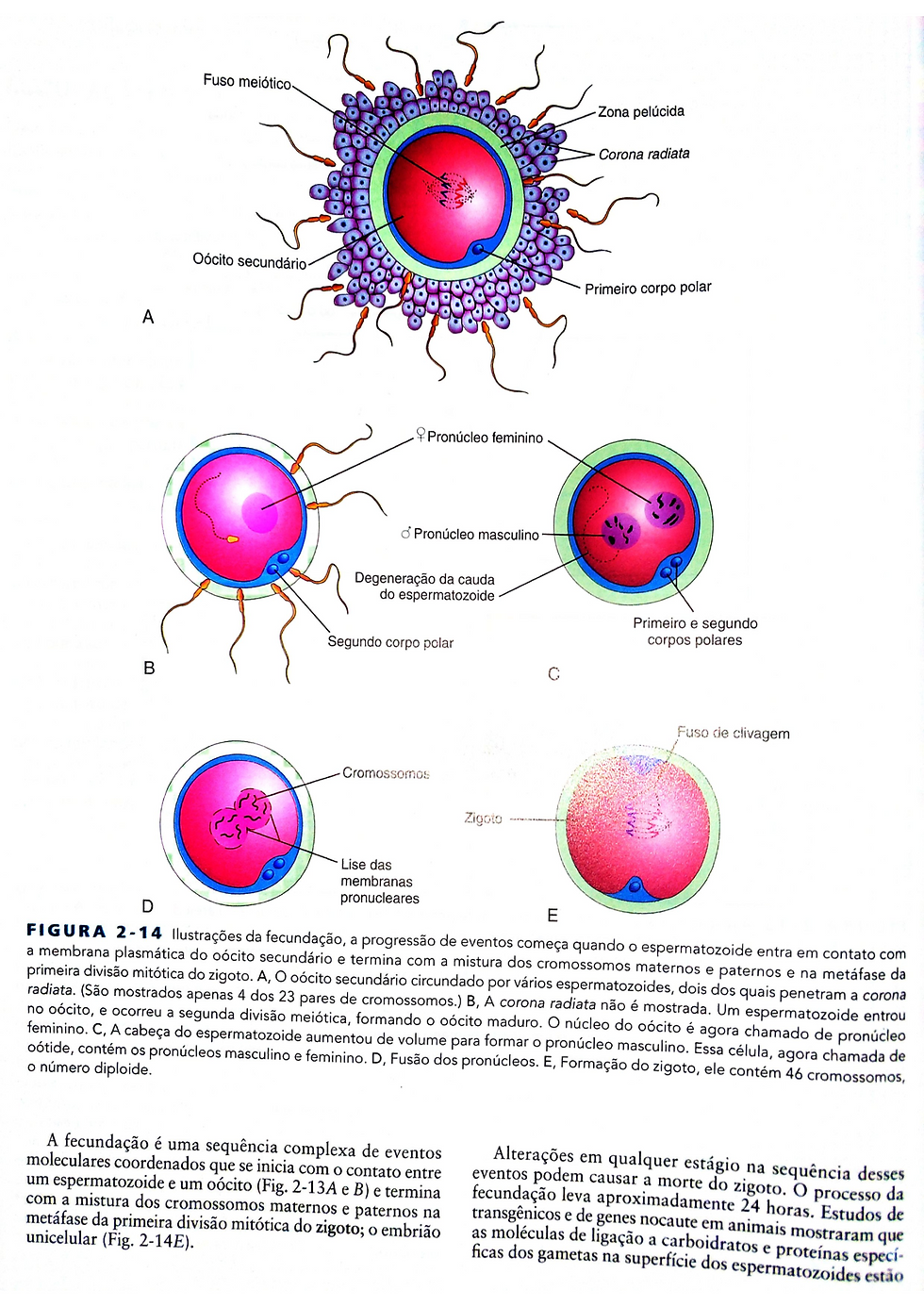
5- término da segunda divisão meiótica do oócito e formação do pronúcleo feminino. quando o espermatozóide penetra no oócito Este é ativado e termina a segunda divisão meiótica formando um oócito maduro e um segundo corpo polar. em seguida, os cromossomos maternos se descondensam e o núcleo do oocito se torna o pronúcleo feminino.
6- formação do pronúcleo masculino. dentro do citoplasma do oócito o núcleo do espermatozóide aumenta para formar o pronucleo masculino e a cauda do espermatozóide degenera. morfologicamente os produtos masculinos e femininos são indistinguíveis. durante o crescimento dos pronúcleos eles replicam seu DNA. o oócito contendo os dois pronúcleos haplóides é dominado oótide.
Logo que os pronúcleos se fundem em um único agregado de cromossomos, a oótide se torna um zigoto.
CLIVAGEMEM DO ZIGITO
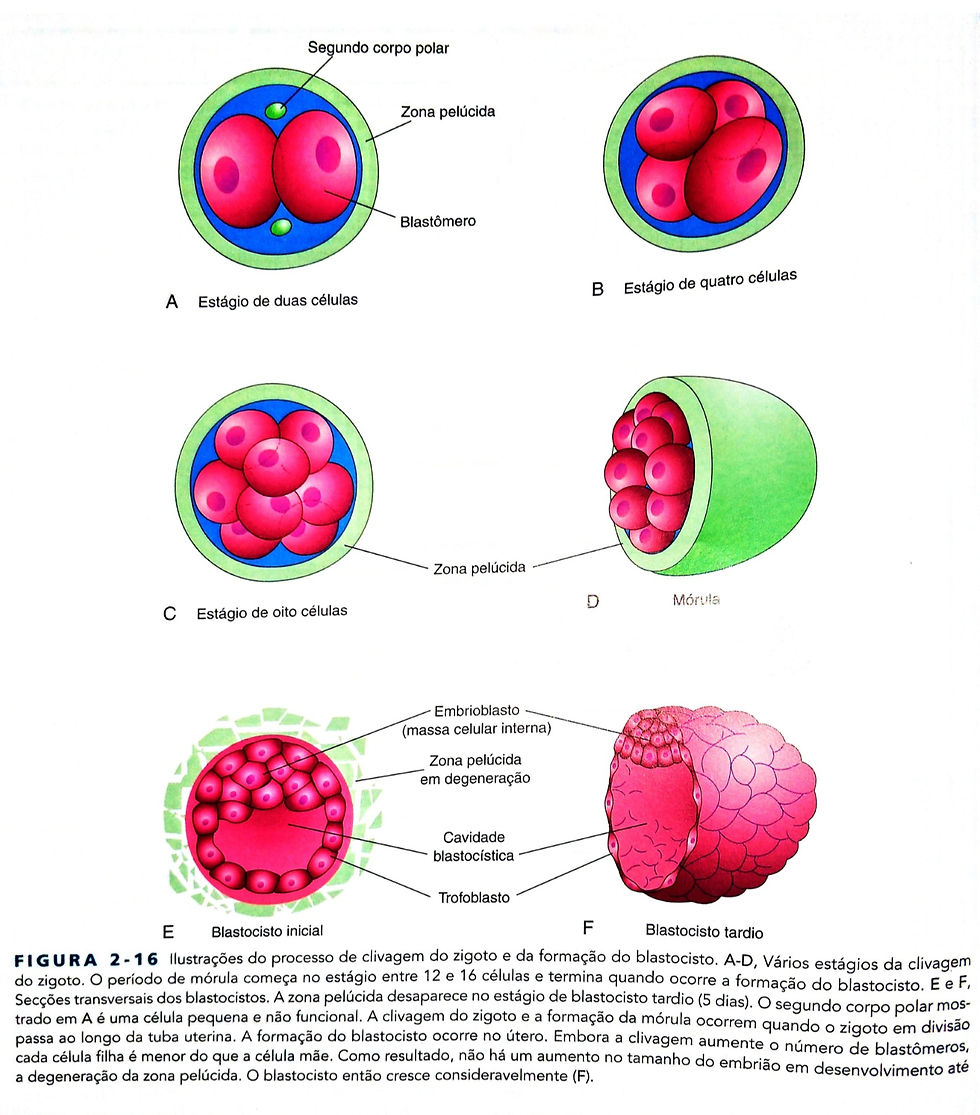
A clivagem consiste em divisões mitóticas repetidas do zigoto, resultando em um aumento rápido do número de células (blastômeros). essas células embrionárias tornam-se menores a cada divisão. a clivagem ocorre conforme o zigoto passa pela tuba uterina em direção ao útero. durante a clivagem, o zigoto continua dentro da zona pelucida. a divisão do zigoto em blastomeros e inicia aproximadamente 30 horas após a fecundação. as divisões subsequentes seguem-se uma após a outra, formando, progressivamente blastomeros menores. após o estágio de nove células, os blastomeros mudam sua forma e se agrupam firmemente uns com os outros para formar uma bola compacta de células. Esse fenômeno, a compactação, é provavelmente mediado por glicoproteínas de adesão de superfície celular. A compactação possibilita uma maior interação célula-célula e é um pré-requisito para a separação das células internas que formam o embrioblasto ( massa celular interna) do blastocisto.

NOVA SÍNTESE:
--Natural:
-espermatozoide passa pela coroa radiada, depois penetra a zona pelúcida.
-Fusão das membranas
-Termina 2ª divisão meiótica
-Formação dos pró-núcleos e sua fusão
-primeira divisão mitótica
-Taxa de sucesso: 20/25%
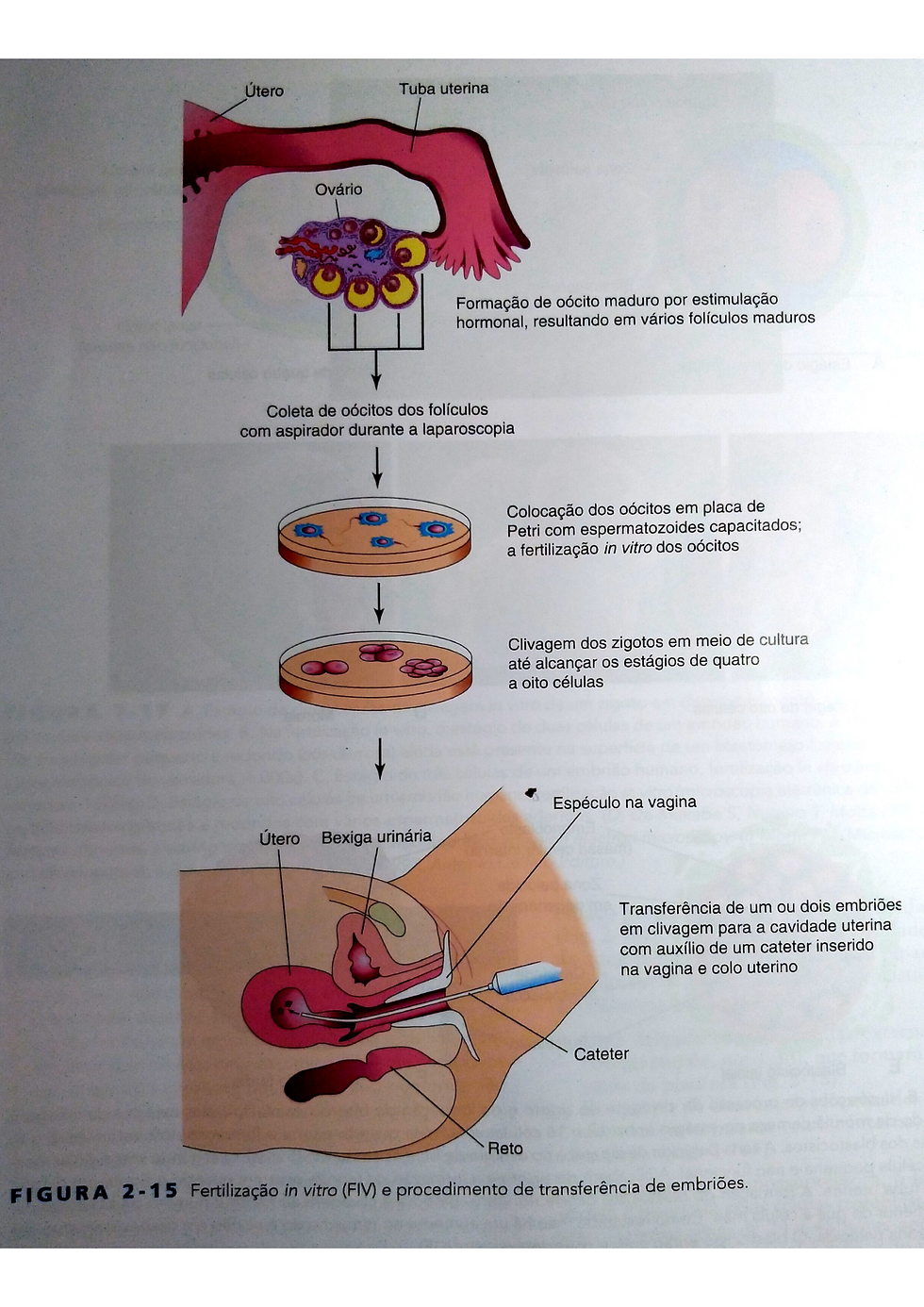
--In Vitro
-super ovulação por estímulos hormonais
-retirada dos ovócitos por laparoscopia
-colocado em meio de cultura com espermatozoides capacitados
-fecundação
-pós estágios de 8 blastômeros coloca-se o embrião no útero
-Taxa de sucesso: 5/50%
REFERÊNCIAS:
Livro : Embriologia Clínica por Moore
QUESTÃO 5
A Organização Mundial da Saúde definiu que infertilidade é a incapacidade de um casal conseguir engravidar após um ano de relação sexual sem a utilização de métodos contraceptivos.
Infertilidade Feminina
Infertilidade é a dificuldade de um casal obter gravidez no período de um ano tendo relações sexuais sem uso de nenhuma forma de anticoncepção. As causas de infertilidade ligadas ao fator feminino podem ser divididas em quatro grupos:
- causas ovarianas e ovulares:
Síndrome dos ovários policísticos ou síndrome da anovulação (ausência de ovulação) crônica; insuficiência ovariana prematura ou menopausa precoce; secreção excessiva de prolactina; hipotireoidismo; idade da mulher – basicamente, a partir dos 37 anos;
- causas tubárias e do canal endocervical:
Obstrução tubária, geralmente provocada pela endometriose ou infecções pélvicas; alterações na secreção do muco cervical;
- causas ligadas à fertilização:
Vigor do espermatozoide e do óvulo; defeitos nos cromossomos ou nas outras estruturas que regulam a fusão dos dois gametas não permite a fertilização; exposição a fatores de risco (raios X, radiações, medicamentos tóxicos) podem dificultar ou impedir a fertilização; idade da mulher;
- causas ligadas à implantação do embrião:
A implantação é a penetração do embrião na camada que reveste a cavidade uterina, chamada endométrio. Esse revestimento é preparado para receber o embrião formado após a ovulação e fertilização. Os hormônios femininos (estrógeno e progesterona) são responsáveis pela preparação do endométrio, durante o ciclo menstrual. Portanto, falhas hormonais podem produzir um endométrio inadequado para a implantação.

Infertilidade Masculina
Infertilidade é a dificuldade de um casal obter gravidez no período de um ano tendo relações sexuais sem o uso de nenhuma forma de anticoncepção. Estima-se que a infertilidade atinja 10% a 20% dos casais em idade reprodutiva, independentemente de suas origens étnicas ou sociais. Em aproximadamente 30% dos casos, a infertilidade é causada apenas por fatores masculinos.
Causas:
- criptorquidia (testículos que não desceram): malformação identificada no nascimento do menino, caracterizada pelo posicionamento incorreto do testículo, atrapalhando a produção de espermatozoides. O problema deve ser corrigido na infância para evitar a infertilidade;
- fatores genéticos;
- fatores hormonais;
- infecções, como prostatites, uretrites, infecções urinárias;
- obstrução do canal por onde passam os espermatozoides;
- varicocele (veias do testículo com dilatação anormal);
Outros fatores: radioterapia, quimioterapia, doenças neurológicas, diabetes, traumas testiculares, drogas, doenças sexualmente transmissíveis.


NOVA SÍNTESE:
A Organização Mundial da Saúde definiu que infertilidade é a incapacidade de um casal conseguir engravidar após um ano de relação sexual com 2 ou + relações sexuais por semana sem a utilização de métodos contraceptivos.
--Feminino
- causas ovarianas e ovulares:
- causas tubárias e do canal endocervical:
- causas ligadas à fertilização:
- causas ligadas à implantação do embrião:
--Masculinas
- criptorquidia (testículos que não desceram): malformação identificada no nascimento do menino, caracterizada pelo posicionamento incorreto do testículo, atrapalhando a produção de espermatozoides. O problema deve ser corrigido na infância para evitar a infertilidade;
- fatores genéticos;
- fatores hormonais;
- infecções, como prostatites, uretrites, infecções urinárias;
- obstrução do canal por onde passam os espermatozoides;
- varicocele (veias do testículo com dilatação anormal);
-Álcool, droga e tabagismo
-Idade avançada
Outros fatores: radioterapia, quimioterapia, doenças neurológicas, diabetes, traumas testiculares, drogas, doenças sexualmente transmissíveis.
--Casal
-Alimentação
-Rotina
-Atividade física
-Há especulação de que a mulher pode produzir anticorpos contra o espermatozoide do homem
REFERÊNCIAS:
Ministério da Saúde - Biblioteca Virtual em Saúde - 23/02/2015 - Infertilidade Feminina - http://bvsms.saude.gov.br/dicas-em-saude/151-infertilidade-feminina
Ministério da Saúde - Biblioteca Virtual em Saúde - 23/02/2015 - Infertilidade Masculina - http://bvsms.saude.gov.br/dicas-em-saude/152-infertilidade-masculina
José Luís Silva Carvalho - Infertilidade - Capitulo 28 - http://www.fspog.com/fotos/editor2/cap_28.pdf
QUESTÃO 6
A cronologia da diferenciação sexual cursa com o estabelecimento do sexo cromossômico, seguido do desenvolvimento gonadal que desencadeará o desenvolvimento do sexo fenotípico.
Na primeira fase do desenvolvimento embrionário, as gônadas são consideradas indiferenciadas ou bipotenciais sendo chamadas assim por não apresentarem diferença histológica entre uma gônada masculina de uma gônada feminina. Porém, a presença do cromossomo Y no genoma do embrião na 7ª semana da gestação é que vai fazer com que os testículos se desenvolvam a partir da gônada indiferenciada, processo mediado pelo gene localizado no cromossomo Y, na designada região do cromossomo Y determinante do sexo (SRY); a identificação da região determinante do sexo no cromossomo Y (gene SRY) constitui uma etapa crucial na compreensão da determinação do sexo gonadal masculino.
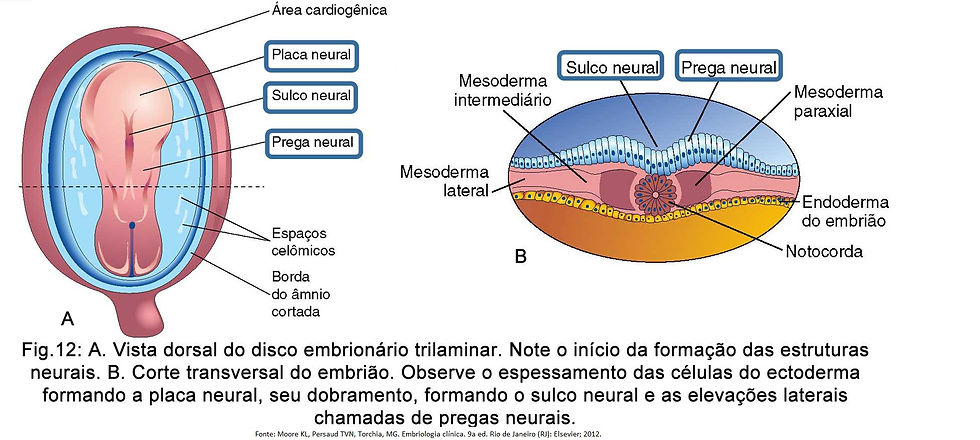
No início do desenvolvimento embrionário, tanto as gônadas como as vias urogenitais não são diferentes em embriões com genótipo masculino ou feminino. Durante a fase indiferenciada, os embriões do sexo masculino e do sexo feminino apresentam dois pares de canais chamados de par de canais Mulleriano e o par de canais Wolffiano.
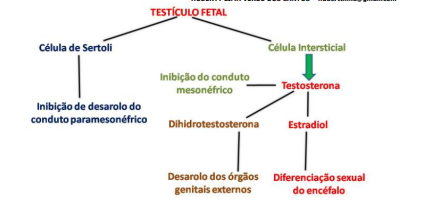
Os testículos começam a se desenvolver devido à presença do cromossomo Y, produzindo hormônios específicos do sexo masculino, fazendo a diferenciação. Os mediadores hormonais para a diferenciação são androgênios (produzidos pelas células de Leydig) e o hormônio anti-Mulleriana (produzida pelas células de Sertoli). Ao nível de androgênios, os canais Wolffianos diferenciam-se em epidídimo, canal deferente, vesículas seminais e canais ejaculadores. Já a nível de hormônio anti-Mulleriana, os canais Mullerianos degeneram.
Para que os androgênios atuem na diferenciação sexual é preciso que se tenha presença de receptores de androgênios nas células-alvo. Quando não ocorrem os hormônios testiculares, os canais wolffianos diminuem e os canais Mullerianos dão origem as trompas uterinas, útero e vagina.
Quando o feto é feminino, os ductos de Müller dão origem a tuba uterina, útero e vagina cranial.
No feto masculino, através da ação local da testosterona secretada pelas células de Leydig, os ductos de Wolff se diferenciam em epidídimo, ducto deferente e vesícula seminal; e os ductos de Müller sofrem atrofia sob ação do hormônio antimülleriano (HAM), secretado pelas células de Sertoli.
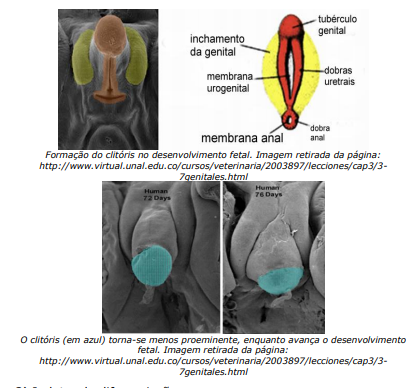
Os genitais externos, na mulher o tubérculo genital dá origem ao clitóris; as pregas urogenitais em pequenos lábios, as pregas lábio-escrotais em grandes lábios e o seio urogenital na porção inferior da vagina.
Diferenciação da Genitália Masculina:
O embrião torna-se do sexo masculino devido presença do cromossomo Y conforme já explicado anteriormente, porém é o gene SRY que vai determinar a produção gonadal no caso o testículo.
As células germinativas endodérmicas (surgem a partir do saco vitelínico) migram para a crista genital; se organizando formando os cordões sexuais. O gene SRY faz com que as células germinativas gerem as células de Sertoli, os túbulos seminíferos e a rede testicular. As células de Sertoli produzem HIM (Hormônio Inibidor Mülleriano), hormônio este que determina a regressão dos ductos de Müller, o que irá originar uma formação vestigial (útero masculino). As células de Leydig produzem testosterona responsável pela manutenção dos Dutos de Wolff que irão dar origem ao epidídimo e aos ductos deferentes.
A Testosterona é transformada em Dihidrotestosterona (DHT) através da enzima. É o DHT que fará a diferenciação da genitália externa masculina.
Sinus urogenital (uretra, glândulas anexas)
Tubérculo genital (pênis e prepúcio)
Pregas genitais (escroto)
Diferenciação da Genitália Feminina
Neste caso não se tem o gene SRY, porque o sexo é feminino. As células germinativas (cordões epiteliais) darão origem às células foliculares. As células mesenquimais (crista genital) darão origem às células da teca. Como não há o gene SRY que acaba gerando as células de Sertoli que é responsável por produzir o hormônio Inibidor Mülleriano, logo não poderemos ter também a produção desse hormônio, então os dutos de Müller irão originar a tuba uterina, útero e vagina cranial.
Não há produção de testosterona e DHT, então a diferenciação da genitália externa feminina será:
Sinus urogenital (vagina caudal e uretra)
Tubérculo genital (clitóris)
Pregas genitais (lábios vulvares)
NOVA SÍNTESE:
-Após a 7ª semana
-Realizada pela presença ou não do cromossomo y
-Gene SRY (no cromossomo y) ativa um potencializador especifico de testículo
- ausência do cromossomo y resulta na formação do ovário
REFERÊNCIAS:
PROF: LIMA VERDE, HUBERTT - BIOLOGIA REPRODUÇÃO E EMBRIOLOGIA - UFPA - file:///C:/Users/Renata%20Jashchenko/Desktop/AULA%2008%20-%20DETERMINA%C3%87%C3%83O%20E%20DIFERENCIA%C3%87%C3%83O%20SEXUAL%20HUMANA%20-%20PARTE%2002.pdf
DETERMINAÇÃO DO SEXO E DESENVOLVIMENTO DOS ÓRGÃOS SEXUAIS - ROSA, Bruna Regina Teixeira da, FERREIRA, Manoela Maria Gomes, MARTINS, Irana Silva - FAMED - 2009 - http://faef.revista.inf.br/imagens_arquivos/arquivos_destaque/VfWNFFiJ7oaCDWl_2013-6-21-10-42-0.pdf
DETERMINAÇÃO SEXUAL E DIFERÊNCIAÇÃO SEXUAL NO EMBRIÃO E NO FETO - UFRGS - 2004 - https://www.ufrgs.br/lacvet/restrito/pdf/difer_sexual.pdf



Comentários