NCS: metabolismo de lipídeos, colesterol, ateroma, síndrome metabólica
- ReMed

- 10 de jan. de 2021
- 14 min de leitura
1ano 1semestre 3módulo 3SP
15 de Maio de 2019


QUESTÕES
CONCEITUE LIPÍDIOS ( O QUE É, QUAIS ) E EXPLIQUE SEU METABOLISMO
CARACTERIZE COLESTEROL ( O QUE É, QUAIS SÃO) E COMO ELES SE RELACIONAM
COMO O CORTISOL (glicocorticoides) AFETA NO METABOLISMO DOS LIPÍDEOS E COMO O CORTISOL SE RELACIONA COM O ESTRESSE CRÔNICO
CORRELACIONE TABAGISMO COM ATEROMA
COMO A OBESIDADE SE RELACIONA COM A RESISTÊNCIA A INSULINA E A ALTA GLICEMIA?
1. CONCEITUE LIPÍDIOS ( O QUE É, QUAIS ) E EXPLIQUE SEU METABOLISMO C, F
Lipídios moléculas orgânicas são formadas a partir da associação entre ácidos graxos e álcool. Não são solúveis em água, mas se dissolvem em solventes orgânicos, como a benzina e o éter. Apresentam coloração esbranquiçada ou levemente amarelada.
Os lipídios são classificados em simples, compostos e derivados.
Os lipídios simples são compostos que por hidrólise total dão origem somente a ácidos graxos e álcoois. Esta categoria inclui os óleos e gorduras, representados pelos ésteres de ácidos graxos e glicerol, sendo denominados acilgliceróis; e as ceras, ésteres de ácidos graxos e monohidroxiálcoois de alto peso molecular geralmente de cadeia linear.
Os lipídios compostos são aqueles que contêm outros grupos na molécula, além de ácidos graxos e alcoóis. Este grupo inclui os fosfolipídios (ou fosfatídios), que consistem de ésteres de ácidos graxos, que contêm ainda na molécula ácido fosfórico e um composto nitrogenado; e os cerebrosídios (ou glicolipídios), compostos formados por ácidos graxos, um grupo nitrogenado e um carboidrato.
São chamados lipídios derivados as substâncias obtidas na sua maioria por hidrólise dos lipídios simples e compostos. Este grupo inclui ácidos graxos; alcoóis, como glicerol, alcoóis de cadeia reta de alto peso molecular, e esteróis; hidrocarbonetos; vitaminas lipossolúveis; pigmentos; e compostos nitrogenados, entre os quais colina, serina, esfingosina e aminoetanol. (1)

METABOLISMO


A. Processamento dos lipídeos da dieta no estômago
A digestão dos lipídeos começa no estômago, catalisada por uma lipase estável em meio ácido (lipase lingual) que se origina de glândulas locali-
zadas na base da língua. As moléculas de TAG, particularmente aquelas que contêm ácidos graxos de cadeia curta ou média (com menos de 12 carbonos, como os encontrados na gordura do leite), são os alvos prin-cipais dessa enzima. Esses mesmos TAGs são degradados também por outra lipase, a lipase gástrica, secretada pela mucosa gástrica.
B. Emulsificação dos lipídeos da dieta no intestino delgado
O processo crítico de emulsificação dos lipídeos da dieta ocorre no duodeno. A emulsificação aumenta a área da superfície das gotículas de lipídeos hidrofóbicos, de maneira que as enzimas digestivas, as quais trabalham na interface da gotícula com a solução aquosa que a envolve, possam agir com eficiência. A emulsificação é obtida por dois mecanismos complementares, a saber, o uso das propriedades detergentes dos sais biliares e a mistura mecânica devida ao peristaltismo.
C. Degradação dos lipídeos da dieta por enzimas pancreáticas
Os TAG, ésteres de colesterol e fosfolipídeos da dieta são degradados enzimaticamente (“digeridos”) por enzimas pancreáticas, cuja secreção é hormonalmente controlada.
1. Degradação de TAG.
As moléculas de TAG são muito grandes para serem captadas eficientemente pelas células mucosas das vilosidades intestinais. Portanto, elas sofrem a ação de uma esterase, a lipase pancreática, que remove ácidos graxos preferencialmen- te dos carbonos 1 e 3. Assim, os principais produtos da hidrólise são uma mistura de 2-monoacilglicerol e ácidos graxos livres.
Uma segunda proteína, a colipase, também secretada pelo pâncreas, liga-se à lipase na razão de 1:1 e a ancora na interface lipídeo-água. A colipase restabelece a atividade da lipase na presença de substâncias inibidoras, como os ácidos biliares que ligam as micelas.
2. Degradação de ésteres de colesterol.
A maior parte do colesterol da dieta está presente na forma livre (não esterificado), com 10 a 15% presentes na forma esterificada. Os ésteres de colesterol são hidrolisados pela hidrolase dos ésteres de colesterol (colesterol- esterase) pancreática, que produz colesterol e ácidos graxos livres. A atividade da hidrolase dos ésteres de colesterol é muito aumentada na presença de sais biliares.
3. Degradação de fosfolipídeos. O suco pancreático é rico na pró-enzima da fosfolipase A2 que, como a pró-colipase, é ativada pela tripsina e, como a hidrolase dos ésteres de colesterol, necessita de sais biliares para sua atividade ótima. A fosfolipase A2 remove um ácido graxo do carbono 2 de um fosfolipídeo, originando um lisofosfolipídeo. Por exemplo, a fosfatidilcolina (o fosfolipídeo predominante durante a digestão) torna-se lisofosfatidilcolina. O ácido graxo que resta no carbono 1 pode ser removido pela lisofosfolipase, originando a base glicerilfosforil (p. ex., glicerilfosforilcolina) que pode ser posteriormente degradada, absorvida ou excretada nas fezes.
4. Controle da digestão dos lipídeos. A secreção pancreática das enzi- mas hidrolíticas que degradam os lipídeos da dieta no intestino delga- do é controlada hormonalmente. As células na mucosa do duodeno inferior e do jejuno produzem um pequeno hormônio pep- tídico, a colecistocinina (CCK), em resposta à presença de lipídeos e de proteínas parcialmente digeridas que entram nessas regiões do in- testino delgado superior. A CCK age sobre a vesícula biliar (fazendo-a contrair-se e liberar a bile – uma mistura de sais biliares, fosfolipídeos e colesterol livre) e sobre as células exócrinas do pâncreas (fazendo- -as liberar enzimas digestivas). Ela diminui também a motilidade gás- trica, resultando na liberação mais lenta dos conteúdos gástricos no intestino delgado. Outras células intestinais produzem outro pequeno hormônio peptídico, a secretina, em resposta ao baixo pH do quimo ao entrar no intestino. A secretina induz o pâncreas e o fígado a liberarem uma solução aquosa rica em bicarbonato, que ajuda a neutralizar o pH do conteúdo intestinal, trazendo-o para o pH apropriado para a atividade digestiva das enzimas pancreáticas.
D. Absorção de lipídeos pelas células da mucosa intestinal (enterócitos)
Ácidos graxos livres, colesterol livre e 2-monoacilglicerol são os princi- pais produtos da digestão dos lipídeos no jejuno. Estes, juntamente com os sais biliares e as vitaminas lipossolúveis (A, D, E e K), formam as micelas mistas – agregados em forma de disco de lipídeos anfipáticos, que coalescem com os seus grupos hidrofóbicos para o interior e seus grupos hidrofílicos para a superfície. As micelas mistas são, portanto, solúveis no meio aquoso do lúmen intestinal . Estas partículas se aproximam do principal local de absorção de lipídeos, a membrana com borda em escova dos enterócitos (células da mucosa). Esta membrana é separada dos conteúdos líquidos do lúmen intestinal por uma camada aquosa estacionária que se mistura pouco com o fluido total. A superfície hidrofílica das micelas facilita o transporte dos lipídeos hidrofóbicos através da camada de água estacionária para a membrana com borda em escova, onde eles são absorvidos. Os sais biliares são absorvidos no íleo. [Nota: em relação a outros lipídeos da dieta, o colesterol é muito pouco absorvido pelos enterócitos. A terapia farmacológica (p. ex., com ezetimiba2) pode reduzir ainda mais a absorção de colesterol no intestino delgado.] Ácidos graxos com cadeias curta e média não necessitam da participação de micelas mistas para sua absorção pela mucosa intestinal.
E. Ressíntese de TAG e ésteres de colesterol
A mistura de lipídeos absorvida pelos enterócitos migra para o retículo endoplasmático, onde ocorre a biossíntese de lipídeos complexos. Os áci- dos graxos são primeiro convertidos em sua forma ativada pela sintetase dos acil-CoA graxos (tiocinase) (Figura 15.6). Usando derivados acil-CoA graxos, os 2-monoacilgliceróis absorvidos pelos enterócitos são convertidos
em TAGs pelo complexo enzimático sintase dos TAG. Esse complexo sintetiza TAG pela ação consecutiva de duas atividades enzimáticas – acil-CoA:monoacilglicerol-aciltransferase e acil-CoA:diacilglicerol-acil- transferase. Os lisofosfolipídeos são reciclados para formar fosfolipídeos por uma família de aciltransferases, e o colesterol é esterificado com um ácido graxo, principalmente pela acil-CoA:colesterol-aciltransferase.
(Nota: praticamente todos os ácidos graxos de cadeia longa que entram nos enterócitos são usados dessa maneira para formar TAGs, fosfolipídeos e ésteres de colesterol. Os ácidos graxos de cadeia curta e média não são convertidos em seus derivados CoA e não são reeste- rificados ao 2-monoacilglicerol. Em vez disso, eles são liberados para a circulação porta, sendo carregados pela albumina sérica para o fígado.)


F. Secreção de lipídeos a partir dos enterócitos Os TAGs e os ésteres de colesterol novamente sintetizados são muito hidrofóbicos, e agregam-se em meio aquoso. Portanto, é necessário que eles sejam embalados como partículas, na forma de pequenas gotas de gordura circundadas por uma fina camada, composta de fosfolipídeos, colesterol não esterificado e uma molécula da proteína característica apolipoproteína B-48 (veja a p. 228). Essa camada estabiliza a partícula e aumenta a sua solubilidade, evitando, assim, que muitas partículas coalesçam. (Nota: a proteína microssomal transferidora de TAG é essencial para a formação dessas partículas lipoproteicas ricas em TAG contendo apolipoproteína B no retículo endoplasmático.) As partículas são liberados por exocitose dos enterócitos para os lactélios (vasos linfáticos que se originam nas vilosidades do intestino delgado). A presença dessas partículas na linfa após uma refeição rica em lipídeos dá à linfa uma aparência leitosa. Essa linfa é chamada quilo (em oposição ao quimo – o nome dado para a massa semifluida de ali- mento parcialmente digerido que passa do estômago para o duodeno), e as partículas são chamadas quilomicra. Os quilomicra seguem pelo sistema linfático até o ducto torácico e são, em seguida, transportados para a veia subclávia esquerda, onde entram no sangue.
G. Utilização dos lipídeos da dieta pelos tecidos
Os triacilgliceróis presentes nos quilomicra são hidrolisados principal- mente nos capilares do músculo esquelético e do tecido adiposo, mas também nos capilares do coração, dos pulmões, dos rins e do fígado. O triacilglicerol presente nos quilomicra é degradado a ácidos graxos livres e glicerol pela lipase lipoproteica. Essa enzima é sintetizada principal- mente pelos adipócitos e pelas células musculares. Ela é secretada e se torna associada à superfície luminal das células endoteliais dos leitos capilares dos tecidos periféricos. (Nota: a deficiência familiar da lipase lipoproteica [hiperlipoproteinemia do tipo I] é uma rara doença autossô- mica recessiva causada por uma deficiência da lipase lipoproteica ou de sua coenzima, a apolipoproteína C-II, o resultado é quilo- micronemia e hipertriacilglicerolemia de jejum.
1. Destino dos ácidos graxos livres. Os ácidos graxos livres derivados da hidrólise dos TAGs podem entrar diretamente tanto nas células musculares adjacentes como nos adipócitos, ou podem ser transportados no sangue em associação com a albumina sérica até serem captados pelas células. (Nota: a albumina sérica é uma pro- teína grande secretada pelo fígado. Ela transporta diversos com- postos, basicamente hidrofóbicos, no sistema circulatório, incluindo ácidos graxos livres e alguns fármacos.) Muitas células podem oxi- dar ácidos graxos para produzir energia (veja a p. 190). Os adipóci- tos podem também reesterificar ácidos graxos livres para produzir moléculas de TAG, as quais são armazenadas até os ácidos graxos serem necessários para o corpo
2. Destino do glicerol. O glicerol liberado a partir dos TAGs é utilizado quase exclusivamente pelo fígado para produzir glicerol-3-fosfato, que pode entrar tanto na glicólise como na gliconeogênese, por oxi- dação a di-hidroxiacetona-fosfato (veja a p. 190).
3. Destinos dos demais componentes dos quilomicra. Após a remoção da maior parte dos TAGs, os quilomicra remanescentes (que contêm ésteres de colesterol, fosfolipídeos, apolipoproteínas, vitaminas lipossolúveis e alguns TAG) ligam-se a receptores no fí- gado (veja a p. 230) e sofrem, então, endocitose. A seguir, os re- manescentes são hidrolisados em seus constituintes. O colesterol e as bases nitrogenadas dos fosfolipídeos (p. ex., a colina) podem ser reciclados pelo corpo. (Nota: se a remoção dos remanescentes pelo fígado estiver diminuída por uma deficiência na ligação ao seu receptor, eles se acumulam no plasma. Isso é observado na hiper- lipoproteinemia do tipo III [uma condição rara, também chamada disbetalipoproteinemia familiar.

(2)
NOVA SÍNTESE:

REFERÊNCIAS:
(1) OS LIPÍDIOS E SUAS PRINCIPAIS FUNÇÕES, FOOD INGREDIENTS BRASIL Nº 37 - 2016 - http://revista-fi.com.br/upload_arquivos/201606/2016060492601001465239502.pdf
(2)Livro: Bioquímica Ilustrada - Harvey e Ferrier
2. CARACTERIZE COLESTEROL ( O QUE É, QUAIS SÃO) E COMO ELES SE RELACIONAM B, D

Com aparência e textura de uma cera macia, o colesterol é um composto químico da família do álcool, essencial à vida. Sintetizado pelo fígado no que se refere à maior parte que o organismo necessita, seu restante é adquirido através dos alimentos ingeridos. Tanto as taxas de colesterol muito altas quanto as muito baixas são perigosas à saúde. Por ser solúvel apenas em gorduras, o colesterol tem de ser transportado pelo sangue através das seguintes lipoproteínas: VLDL (também conhecidas como triglicérides), LDL (mau colesterol) e HDL (bom colesterol). O fígado acondiciona os triglicérides na forma de VLDL e os despacha, pela corrente sanguínea para as células, juntamente com menores quantidades de colesterol e proteínas. É então que as células armazenam e utilizam essa quantidade de gorduras como "combustível". Assim, o VLDL, sem as gorduras, passa a ser denominado como LDL, já que é composto basicamente de colesterol e proteínas. Seu excesso no organismo, acaba fixando-se nas paredes das artérias, entupindo-as e propiciando os ataques cardíacos ou infartos. Por sua vez, o HDL faz o papel contrário, extraindo o colesterol das paredes das artérias, devolvendo-o ao fígado para ser excretado. O fumo baixa os níveis de HDL, enquanto o exercício físico aumenta. (1) “Sabemos que [o colesterol] é benéfico para determinadas funções vitais e tem participação fundamental na construção e manutenção das membranas celulares; participação na fabricação da bile e é através dos ácidos biliares o único meio significativo pelo qual o colesterol pode ser excretado; é fundamental no metabolismo das vitaminas lipossolúveis A, D, E e K e é responsável pela síntese de hormônios esteroides. É o precursor de todas as classes de hormônios esteroides; glicocorticoides (cortisol), mineralocorticoides (aldosterona) e hormônios sexuais”, (2)

Metabolismo da VLDL e da LDL. TAG = triacilglicerol; VLDL = lipoproteína de densidade muito baixa; LDL = lipoproteína de densidade baixa; IDL = lipoproteína de densidade intermediária; C = colesterol; EC = éster de colesterol. Apo B-100, apo C-II e apo E são apolipoproteínas encontradas como componentes específicos das lipoproteínas plasmáticas. As lipoproteínas não estão desenhadas em escala (veja a Figura 18.13 para detalhes acerca do tamanho e da densidade das lipoproteínas).
NOVA SÍNTESE:

REFERÊNCIAS:
(1) Sociedade Brasileira de Endocrinologia e Metabologia - SBEM - 2007 - https://www.endocrino.org.br/colesterol/
(2) Revista vivendo com saúde, 4 dição - http://www.baruco.com.br/blog/vivendo_com%20saude_ed4.pdf
3. COMO O CORTISOL (glicocorticoides) AFETA NO METABOLISMO DOS LIPÍDEOS E COMO O CORTISOL SE RELACIONA COM O ESTRESSE CRÔNICO A
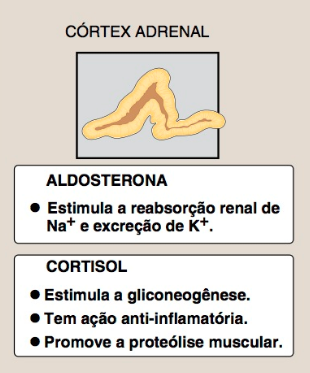
Sua produção na camada média (zona fasciculada) do córtex da adrenal é controlada pelo hipotálamo, junto ao qual está localizada a hipófise.
Em situações de estresse grave (p. ex., uma infecção), o hormônio liberador da corticotropina (CRH), produzido pelo hipotálamo, viaja através da rede de capilares até o lobo anterior da hipófise, onde induz a produção e secreção do hormônio adrenocorticotrópico (ACTH, ou corticotropina).
O ACTH, frequentemente chamado de “hormônio do estresse”, estimula o córtex adrenal a sintetizar e secretar o glicocorticoide cortisol.
O cortisol induz o organismo a responder ao estresse via efeitos sobre o metabolismo intermediário (como, p. ex., pelo aumento da gliconeogênese) e sobre a resposta inflamatória e imunitária. Níveis elevados de cortisol inibem a liberação de CRH e ACTH. (Nota: o ACTH atua em um receptor acoplado à proteína G na membrana plasmática, resultando em produção de AMPc e ativação da proteína-cinase A [veja a p. 94]. A PKA fosforila a esterase que converte os ésteres de colesterol em colesterol e estimula a síntese da proteína esteroidogênica aguda reguladora [StAR].)
NOVA SÍNTESE:

REFERÊNCIAS:
Livro: Bioquímica Ilustrada - Harvey e Ferrier
4. CORRELACIONE TABAGISMO COM ATEROMA E
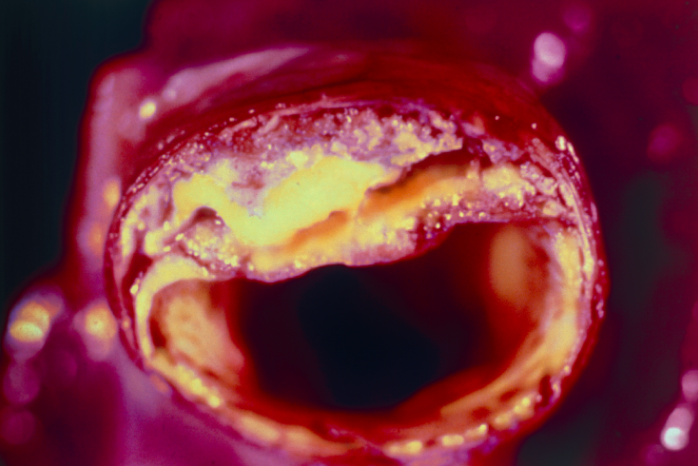
Aterosclerose caracteriza-se por placas intimais irregulares (ateromas) que avançam no lúmem das artérias de médio e grosso calibre; as placas contêm lipídios, células inflamatórias, células musculares lisas e tecido conjuntivo. Os fatores de risco são dislipidemia, diabetes, tabagismo, história familiar, estilo de vida sedentário, obesidade e hipertensão.
Os sintomas surgem quando o crescimento ou a ruptura da placa reduz ou obstrui o fluxo sanguíneo; esses sintomas variam de acordo com a artéria afetada. O diagnóstico é clínico e confirmado por angiografia, ultrassonografia ou outros métodos de imagem. O tratamento abrange modificação de dieta, estilo de vida e fatores de risco, atividade física, drogas antiplaquetárias e antiaterogênicas.
O cigarro contém nicotina e outros produtos químicos que são tóxicos ao endotélio vascular. O tabagismo, incluindo o tabagismo passivo, aumenta a reatividade plaquetária (possivelmente promovendo trombose plaquetária), níveis plasmáticos de fibrinogênio e hematócrito (aumentando viscosidade sanguínea). O tabagismo aumenta a LDL e diminui a HDL, além de promover vasoconstrição, que é especialmente prejudicial às artérias já obstruídas por aterosclerose. A HDL aumenta cerca de 6 a 8 mg/dL (0,16 a 0,21 mmol/L) em 1 mês de interrupção do tabagismo.

Fisiopatologia
A lesão visível mais precoce da aterosclerose é a estria gordurosa, que é o acúmulo de células espumosas carregadas de lipídios na camada íntima da artéria. A característica da aterosclerose é a placa aterosclerótica, que é uma evolução da estria gordurosa e tem três componentes principais:
Lipídios
Células musculares lisas e inflamatórias
A matriz do tecido conjuntivo que pode conter trombos em vários estágios da organização e depósitos de Ca
Todos os estágios da aterosclerose — da iniciação e crescimento à complicação da placa — são considerados uma resposta inflamatória à lesão mediada por citocinas específicas. Considera-se que a lesão endotelial desempenha um papel iniciador ou incitador primário.
A aterosclerose afeta preferencialmente certas áreas da árvore arterial. O fluxo sanguíneo turbulento ou não laminar (p. ex., em pontos de ramificação da árvore arterial) conduz à disfunção endotelial e inibe a produção endotelial de óxido nítrico, uma molécula vasodilatadora e anti-inflamatória potente. Esse fluxo sanguíneo também estimula as células endoteliais a produzir moléculas de adesão, as quais recrutam e se ligam às células inflamatórias. Os fatores de risco de aterosclerose (p. ex., dislipidemia, diabetes, tabagismo e hipertensão), estressores oxidativos (p. ex., radicais superóxidos), angiotensina II, infecção e inflamação sistêmicas também inibem a produção de óxido nítrico e estimulam a produção de moléculas de adesão, citocinas pró-inflamatórias, proteínas quimiotáxicas e vasoconstritores; porém, os mecanismos exatos são desconhecidos. O resultado final é a ligação ao endotélio de monócitos e células T, a migração dessas células ao espaço subendotelial e iniciação e perpetuação de resposta inflamatória vascular local. No subendotélio, os monócitos transformam-se em macrófagos. Os lipídios do sangue, particularmente a LDL e a VLDL, também se ligam às células endoteliais e são oxidados no subendotélio. A captação de lipídios oxidados e a transformação de macrófagos em células espumosas repletas de lipídios resultam nas lesões ateroscleróticas iniciais típicas, denominadas estrias gordurosas. As membranas de eritrócitos degradados que resultam da ruptura de vasa vasorum e da hemorragia dentro da placa podem ser uma fonte adicional de lipídios dentro das placas.
Os macrófagos elaboram citocinas pró-inflamatórias que acarretam a migração de células musculares lisas da média e que, subsequentemente, atraem e estimulam o crescimento de macrófagos. Vários fatores promovem a replicação de células musculares lisas e o aumento da produção de matriz extracelular densa. O resultado é uma placa fibrosa subendotelial com capa fibrosa, composta por células musculares lisas da íntima, circundadas por tecido conjuntivo e lipídios intra e extracelulares. Um processo semelhante à formação óssea provoca calcificação dentro da placa.
As placas ateroscleróticas podem ser estáveis ou instáveis. As placas estáveis regridem, permanecem estáticas ou crescem lentamente ao longo de décadas até que provoquem estenose ou oclusão. As placas instáveis são vulneráveis à erosão, fissura ou ruptura espontâneas, acarretando trombose, oclusão e infarto agudo muito antes de provocarem estenose hemodinamicamente significativa. A maioria dos eventos clínicos resulta de placas instáveis, os quais não parecem graves na angiografia e, por isso, a estabilização da placa pode ser uma maneira de reduzir morbidade e mortalidade.
A rigidez da capa fibrosa e sua resistência à ruptura dependem do equilíbrio relativo de deposição e degradação de colágeno. A ruptura da placa envolve a secreção de metaloproteinases, catepsinas e colagenases por macrófagos ativados na placa. Essas enzimas digerem a capa fibrosa, especialmente nos membros, causando adelgaçamento da capa e, finalmente, a ruptura. As células T da placa contribuem com a secreção de citocinas. As citocinas inibem síntese e deposição de colágeno pelas células musculares lisas, o que normalmente reforça a placa.
Com a ruptura da placa, seus conteúdos são expostos ao sangue circulante, deflagrando trombose; macrófagos também estimulam a trombose porque eles contêm fator tecidual, o que promove a geração de trombina in vivo. Pode ocorrer uma das cinco evoluções:
O trombo resultante pode organizar-se e ser incorporado dentro da placa, modificando seu formato e deflagrando o crescimento rápido.
O trombo pode ocluir rapidamente o lúmen vascular e precipitar um evento isquêmico agudo.
O trombo pode provocar embolia.
A placa pode ser preenchida por sangue, acarretando expansão e oclusão imediata da artéria.
Os conteúdos da placa (em vez de trombos) podem provocar embolia, ocluindo o vaso a jusante.
A estabilidade da placa depende de múltiplos fatores, envolvendo composição (proporção relativa de lipídios, células inflamatórias, células musculares lisas, tecido conjuntivo e trombo), estresse de parede (fadiga da capa), tamanho e localização do núcleo e configuração da placa em relação ao fluxo sanguíneo. Por contribuir para o crescimento rápido e para a deposição de lipídios, a hemorragia dentro da placa pode desempenhar um papel importante na transformação de placas estáveis em instáveis. Em geral, as placas instáveis das artérias coronárias têm conteúdo elevado de macrófagos, núcleo lipídico espesso e capa fibrosa delgada; elas provocam obstrução do lúmen do vaso em < 50% e tendem a se romper imprevisivelmente.
As placas instáveis das artérias carótidas têm a mesma composição, mas classicamente acarretam problemas por estenose e oclusão graves ou deposição de trombos, que se embolizam em vez de romper. Placas de baixo risco têm capa mais espessa e menor conteúdo de lipídios. Geralmente, elas obstruem o lúmen do vaso em > 50% e provocam angina estável induzida por esforço de maneira previsível.
As consequências clínicas da ruptura da placa dependem não somente de sua anatomia, mas também do equilíbrio relativo da atividade pró-coagulante e anticoagulante do sangue e da vulnerabilidade do miocárdio a arritmias.
Sugere-se uma ligação entre infecção e aterosclerose para explicar as associações sorológicas entre infecções (p. ex., Chlamydia pneumoniae, citomegalovírus) e DAC. Outros mecanismos prováveis compreendem efeitos indiretos de inflamação crônica na corrente sanguínea, anticorpos de reação cruzada e efeitos inflamatórios de patógenos infecciosos na parede arterial.
NOVA SÍNTESE:

REFERÊNCIAS:
Aterosclerose - Por Jules Y. T. Lam, MD, FRCP(C), Associate Professor of Medicine, University of Montreal; Cardiologist, Montreal Heart Institute - https://www.msdmanuals.com/pt-br/profissional/dist%C3%BArbios-cardiovasculares/arterioesclerose/aterosclerose
5. COMO A OBESIDADE SE RELACIONA COM A RESISTÊNCIA A INSULINA E A ALTA GLICEMIA? C
A obesidade tem como efeitos predominantes da obesidade incluem dislipidemias, intolerância à glicose (hiperglicemia abaixo daquela classificada como diabetes) e resistência à insulina, expressa principalmente no fígado, no músculo e no tecido adiposo. Essas anormalidades metabólicas refletem sinais moleculares que se originam da massa aumentada de adipócitos.
Síndrome metabólica
A obesidade abdominal está associada a um grupo de anormalidades metabólicas que tem sido chamado de síndrome metabólica, e inclui intolerância à glicose, resistência à insulina, hiperinsulinemia, dislipidemia (baixo nível de lipoproteínas de alta densidade [HDL] e aumento do nível de triacilgliceróis) e hipertensão.
A síndrome metabólica também está associada a um estado de inflamação sistêmica crônica, que contribui para a patogênese da resistência à insulina e para a aterosclerose. Na obesidade, níveis baixos do hormônio adiponectina podem contribuir para a síndrome metabólica e, assim, para o risco de diabetes tipo 2 e de doença cardíaca, pois esse hormônio, produzido no tecido adiposo, normalmente freia a inflamação e aumenta a sensibilidade dos tecidos, especialmente do fígado, à insulina.
NOVA SÍNTESE:

REFERÊNCIAS:
Livro : Bioquímica Ilustrada - Harvey e Ferrier




Comentários